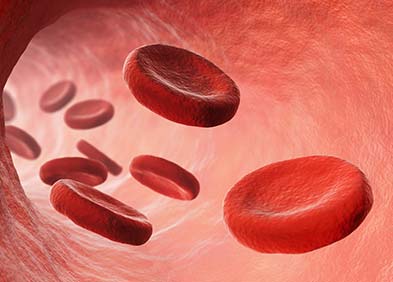
La drépanocytose, aussi appelée anémie falciforme, est une maladie héréditaire touchant l’hémoglobine des globules rouges. Cette protéine est essentielle à la fonction respiratoire: c’est elle qui permet le transport de l’oxygène dans notre organisme. Elle participe aussi à l’élimination du dioxyde de carbone.
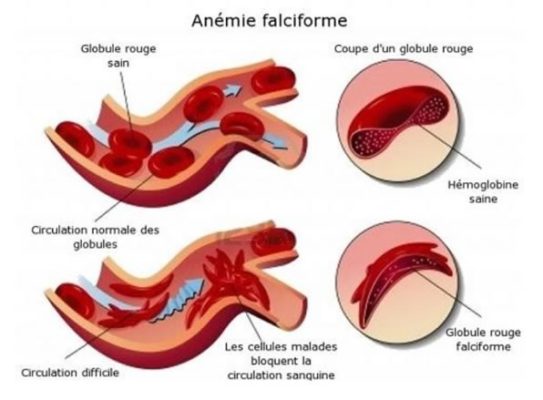
Chez les personnes atteintes de dré panocytose, l‘hémoglobine est anormale. Quand la concentration en oxygène du sang diminue, elle déforme les globules rouges (ou hématie) qui prennent alors la forme de faucilles, au lieu d’être biconcaves. Il en résulte plusieurs symptômes caractéristiques de la maladie dont les plus courants sont une anémie chronique, des crises douloureuses vaso-occlusives et une sensibilité plus importante aux infections.
Cette maladie génétique est très répandue dans le monde. Apparue indépendamment en Afrique et en Inde, elle touche tout particulièrement les populations de ces régions. Mais les mouvements de populations l’ont rendue en outre très présente en Amérique, tout particulièrement aux Antilles et au Brésil, et en Europe de l’Ouest. En France, 441 enfants drépanocytaires ont vu le jour en 2013, soit une prévalence d’un enfant atteint pour 1 900 naissances. Ce chiffre en fait la maladie génétique la plus fréquente en France. Toutefois cette prévalence est beaucoup plus importante dans les départements d’outre-mer (1/419) et en région parisienne (1/874) où se concentrent les populations à risque.
Transmission aux enfants, diagnostic prénatal et préimplantatoire
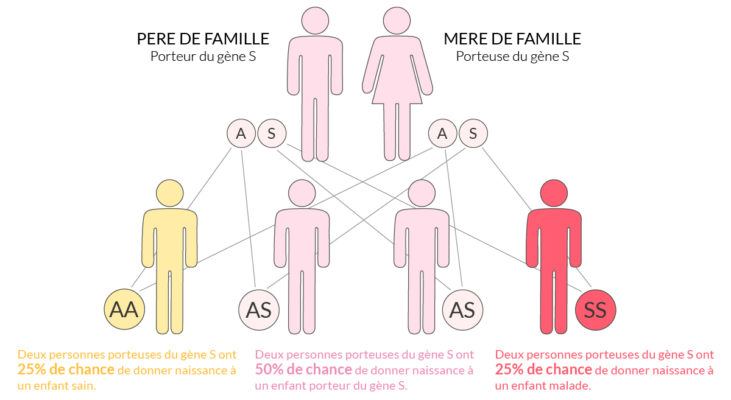
La drépanocytose est une maladie génétique autosomique récessive : pour qu’elle se déclare il faut que chacun des parents transmette un allèle muté à leur enfant. Pour des parents porteurs sains, le risque d’avoir un enfant souffrant de la maladie est donc de un sur quatre. Pour un couple comprenant un drépanocytaire et un porteur sain, le risque est de un sur deux.
En France, un dépistage néonatal est systématiquement réalisé chez les enfants de parents issus des populations les plus concernées par la maladie. Il permet de déterminer si l’enfant est porteur sain ou malade afin de débuter au plus tôt le traitement préventif de l’anémie et des complications infectieuses.
Un diagnostic prénatal peut être proposé lors d’une grossesse chez un couple à risque. Il consiste à rechercher l’allèle muté dans l’ADN fœtal (à partir de cellules du placenta dès la 12e semaine de grossesse ou par amniocentèse vers la 16e semaine). Il est également possible de réaliser un diagnostic préimplantatoire (DPI) sur des embryons obtenus par fécondation in vitro, mais ce procédé est lourd et très encadré juridiquement.
Le diagnostic de la drépanocytose peut être établi par frottis sanguin : les hématies en forme de faucille sont en effet facilement observables au microscope. L’analyse de l’hémoglobine par électrophorèse est une autre option pour poser le diagnostic. Des tests génétiques révélant la présence du gène muté responsable de la maladie sont utilisés pour résoudre certains cas plus complexes.
Les principaux symptômes de la drépanocytose sont l’anémie hémolytique, les crises douloureuses et une sensibilité accrue aux infections. Ils peuvent apparaitre dès l’âge de 4 mois. Cependant ces symptômes varient beaucoup d’un patient à l’autre et leur intensité évolue au fil des années.
Au fil des ans, toutes ces manifestations de la maladie mettent l’organisme à rude épreuve. Les patients sont souvent affectés par un retard de croissance et une puberté plus tardive. Diverses complications chroniques peuvent se déclarer chez l’adulte. Elles sont susceptibles de toucher presque tous les organes notamment le rein (insuffisance rénale), le système ostéo-articulaire (arthrose, ostéoporose), l’œil (hémorragies intraoculaires), le foie, les poumons (hypertension artérielle pulmonaire) ou encore la vésicule biliaire (calculs).
Pour la plupart des patients, la prise en charge de la drépanocytose s’articule autour :
- d’une prévention des complications (administrer préventivement des antibiotiques et à renforcer le programme vaccinal, une bonne hygiène de vie et une alimentation équilibrée sont essentielles, une bonne hydratation est nécessaire, éviter l’exposition à des températures extrêmes ou à des variations importantes de température et éviter les efforts trop intenses liés à la pratique de sports extrêmes et d’endurance sont à proscrire)
- un suivi médical régulier
- les transfusions sanguines
- la greffe de moelle osseuse : le seul traitement curatif disponible actuellement contre la drépanocytose est la greffe de moelle osseuse. Cette moelle contient en effet les cellules souches qui donnent naissance aux cellules sanguines, dont les globules rouges. Concrètement, les cellules souches de la moelle du patient sont détruites et remplacées par celles d’un donneur sain compatible, souvent un frère ou une sœur. Cependant, on ne trouve pas de donneur compatible pour tous les patients. De plus, cette procédure, très lourde et coûteuse, n’est pas totalement dénuée de risques. Elle est réservée aux formes les plus sévères de la maladie.
Les espoirs de la thérapie génique
Les espoirs de guérison se fondent aujourd’hui sur la thérapie génique. Le but de cette technique prometteuse est de « greffer » un gène sain de la bêta-globine dans les cellules souches hématopoïétiques des drépanocytaires. Des essais encourageants ont été réalisés sur des modèles animaux de la maladie. Le premier patient, traité en 2007, n’a plus besoin de transfusion sanguine et sa qualité de vie s’est donc considérablement améliorée. Aux États-Unis, un essai clinique de phase I fondé sur un protocole similaire est en phase préliminaire de développement chez des patients drépanocytaires.
Source : inserm